BÀI 2: MỘT SỐ OXIT QUAN TRỌNG
TIẾT 1
[toc]
I. Canxi oxit
A. Tóm tắt kiến thức Canxi oxit
– Công thức hóa học: CaO.
– Phân tử khối: 56
– Tên gọi thông thường: vôi sống

a) Tính chất vật lý: chất rắn, màu trắng, nhiệt độ nóng chảy khoảng 2585°c.
b) Tính chát hóa học:
– Tác dụng với nước tạo thành canxi hidroxit Ca(OH)2, phản ứng vôi tôi.
CaO + H2O —> Ca(OH)2
– Tác dụng với axit
CaO + H2SO4 —> CaSO4 + H2O
– Tác dụng với oxit axit
CaO + CO2 —> CaCO3
c) ứng dụng
– Dùng trong công nghiệp luyện kim.
– Nguyên liệu cho công nghiệp hóa học.
– Khử chua đất trổng trọt.
– Xứ lí nước thải công nghiệp, sát trùng, diệt nấm.
d) Sản xuất
CaCO3 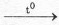 CaO + CO2
CaO + CO2 
TIẾT 2
II. Lưu huỳnh đioxit
A. Tóm tắt kiến thức
Lưu huỳnh đioxit
– Công thức hóa học: SO2
– Phân tử khối: 64
– Tên gọi thông thường: khí sunfurơ
a) Tính chất vật lý
Chất khí không màu, mùi hắc, độc, nặng hơn không khí.
b) Tính chất hóa học
+ Tác dụng với nước tạo thành axit sunfurơ H2SO4
SO2 + H2O -> H2SO4
+ Tác dụng với bazơ.
Ca(OH)2 + SO -> CaSO4 + H2O
+ Tác dụng với oxil bazơ tạo thành muối sunfit (SO2)
CaO + SO2 —> CaSO3
c) ứng dụng
– Sản xuất axit sunfuric: S02 —> so, —> H2S04
– lay trắng bột gỗ trong công nghiệp giấy.
– Diệt nấm, mốc và dùng làm chất bảo quản thực phẩm.
d) Điều chế – sán xuát
– Đicu chế trong phòng thí nghiệm:
+ Na2SO3 + H2SO4 —> Na2SO4 + H2O + SO2 
+ Na2SO4 + 2HCl —> 2NaCl + H2O + SO2
– Sản xuất trong công nghiệp:
+ Đốt lưu huỳnh trong không khí: S + O2—> SO2 
+ Đốt quặng pirit sắt (FeS,): 4FeS2 + 11O2 —> 2Fe2O3 + 8SO2 
Tham khảo phần giải bài tập trong SGK tại đây: Một số oxit quan trọng
